 면역항암 한계 넘은 금속-면역치료 기술 개발 |
최근 항암치료의 패러다임은 환자의 면역체계를 활성화하여 항암면역반응을 통해 암세포를 사멸하는 면역항암제로 전환되고 있다.
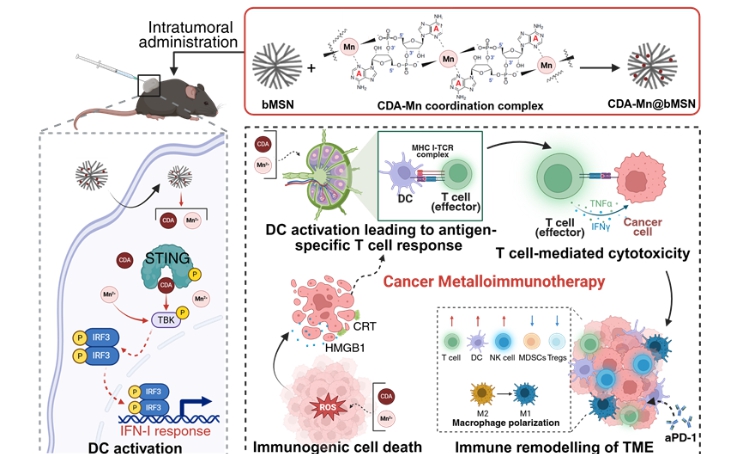
특히 STING(Stimulator of Interferon Genes) 경로를 활성화하는 환형이분자핵산(Cyclic dinucleotide, CDN)이 임상에서 활발하게 연구되고 있지만, 음전하를 띠는 단분자의 한계인 생체에서 쉽게 분해·배출되고 세포막 투과율이 낮다는 치명적인 단점으로 인해 효과가 제한적이었다.
연구진은 이러한 문제를 해결하기 위해 망간 이온(Mn²⁺)과 CDN의 배위결합 복합체를 다공성 실리카 나노입자 내부 기공에 탑재해 망간 이온과 CDN이 활성 제약 성분으로 작용하는 나노-면역항암제를 개발했다.
나노입자의 중요한 설계 요소로서, 체내 필수 미네랄인 망간 이온은 STING 경로의 활성을 증폭시킬 수 있고 생분해가 가능한 다공성 실리카 나노입자를 기반으로 하여 생체친화도를 높였다.
생분해성 실리카 나노입자는 종양 미세환경 내에서 서서히 분해되어 망간과 CDN을 방출하고, 방출된 망간과 CDN은 면역원성 암세포 사멸을 일으킴과 동시에 수지상세포의 STING 경로를 강하게 자극하여 T 세포의 활성을 유발하는 in situ 항암백신 효과를 나타냈다.
또한 in situ 항암백신은 대식세포, NK 세포, MDSC(Myeloid-derived suppressor cell), Treg(Regulatory T cell)을 포함하는 다양한 면역세포의 반응을 조절하여 항암면역반응이 없는 '차가운 종양(Cold tumor)'을 항암면역반응이 활발한 '뜨거운 종양(Hot tumor)'으로 전환시켰다.
흑색종 암모델을 사용한 in vivo 동물실험을 통해 국소 부위의 암이 효과적으로 치료될 뿐만 아니라, 전신면역반응을 유발하여 폐 전이암을 치료하고 암의 재발을 억제하는 효과를 확인했다.
또한 aPD-1 항체 기반의 면역관문억제제와 병용했을 때 항암면역 시너지 반응을 통해 더 효과적으로 국소암 및 폐 전이암을 치료할 수 있다는 것을 확인했다.
본 연구는 생체 친화적인 나노소재를 사용하여 면역치료의 효율을 높일 수 있는 금속-면역치료 나노기술의 가능성을 제시하며, 향후 다양한 의약품의 나노제형 플랫폼으로 활용할 수 있을 것으로 기대된다.
본 연구는 한국연구재단의 중견연구와 한우물파기 기초연구의 지원을 받아 수행됐으며, 연구결과는 “Nanoengineering of cyclic dinucleotide‑manganese complexes using biodegradable mesoporous silica nanoparticles for cancer metallo-immunotherapy"라는 제목으로 Journal of Controlled Release (피인용지수 11.5; JCR 상위 3.3%)에 게재됐다.
 박인석 기자 aihnnews@kakao.com
박인석 기자 aihnnews@kakao.com 2026.05.01 (금) 01:21
2026.05.01 (금) 01:21



































